„An den aktuellen DGI-Leitlinien waren 17 Fachgesellschaften beteiligt“: Prof. Dr. Dr. Knut A. Grötz eröffnete den Kongress unter dem Motto „Implantologie vernetzt“.
Gemeinsamer Kongress von DGI und DGOI spannt Bogen von Periimplantitis und innerer Medizin bis zu digitaler Prothetik
„Implantologie vernetzt“ lautete das Motto des Kongresses, der Ende November 2021 im Wiesbadener Rhein-Main-Congress-Center stattfand. Zum ersten Mal wurde er als Deutscher Implantologentag (DIT) von der Deutschen Gesellschaft für Implantologie (DGI) zusammen mit der Deutschen Gesellschaft für Orale Implantologie (DGOI) sowie der DGI-Nachwuchs-Organisation Nexte Generation gemeinsam ausgerichtet. Neben der US-amerikanischen Academy of Osseointegration (AO) waren auf dem interdisziplinären Kongress die parodontologische (DG Paro) und zwei restaurative (DG Pro, DGÄZ) Fachgesellschaften mit Referenten vertreten, weiterhin die Deutsche Gesellschaft für Innere Medizin (DGIM).
Eine ganze Reihe von Vorträgen lieferte Indizien, dass Periimplantitis vom individuellen Immunstatus abhängt und der Biofilm nicht immer der primäre ätiologische Faktor ist. Denkbar ist eine Analogie zu schwer verlaufenden Parodontitiden, bei denen eine überschießende Immunreaktion auf mikrobiologische Veränderungen vermutet wird.
Für eine wichtige Rolle des Immunsystems sprechen nach Ansicht mehrerer Referenten gemeinsame ätiologische Faktoren zwischen periimplantärer Entzündung und Autoimmunerkrankungen. Die Internistin Prof. Dr. Elisabeth Märker-Hermann (Wiesbaden) erläuterte, dass diese auch mit Allergien oder Unverträglichkeiten verknüpft sind, zum Beispiel über Fremdstoffe wie Implantate oder Implantatpartikel im periimplantären Gewebe. Die darauf gerichtete unspezifische Immunreaktion könnte „Öl auf das Feuer“ einer mikrobiellen Entzündung sein und zugleich das Mikrobiom weiter pathologisch verändern (Prof. Dr. Moritz Kebschull, Birmingham/UK, Workshop Geistlich Biomaterials).Eine ätiologische Rolle könnten nach einer aktuellen Studie auch Verunreinigungen der Implantatoberfläche spielen [1].

„Autoimmunerkrankungen und Titan-Unverträglichkeit scheinen ätiologisch zusammenhängen“ (Prof. Dr. Elisabeth Märker-Hermann).
Zirkonoxidimplantate enthalten Metalle
Mit diesen noch unzureichend belegten Thesen erhält die 2012 mit einem Konsens-Statement begonnene Diskussion über die Ätiologie der Periimplantitis neue Facetten [2]. Hoch interessant sind auch in Wiesbaden präsentierte histologische Befunde von Patientenbiopsien, die sowohl um Titan- als auch um Zirkonoxid-Implantate von diesen stammende Partikel im Gewebe zeigen (PD Dr. Tobias Fretwurst, Freiburg) [3].
Diese sind häufig mit Mukositis und Periimplantitis assoziiert [4]. Eine weitere Arbeitsgruppe demonstrierte anhand chemischer Analysen, dass Zirkonoxidimplantate nicht metallfrei ist, sondern unter anderem Schwermetalle und Radionuklide enthalten (PD Dr. Dr. Andres Stricker, Freiburg, mit Karlsruher Institut für Technologie).
Diskutiert wurde in Bern auch die klinische Beobachtung, dass im Bereich entzündlicher periimplantärer Defekte Plattenepithelkarzinome entstehen können (Prof. Dr. Dr. Peer Kämmerer und Prof. Dr. Dr. Bilal Al-Nawas, beide Universität Mainz). Eine zentrale Rolle spielen könnte hier die chronische Entzündung und damit verknüpfte entgleiste Immunantwort als ätiologischer Faktor für Karzinome. Die angekündigte DGI-Leitlinie zu Materialunverträglichkeiten wird festhalten, dass derzeit keine kausalen Tests für Titan-Unverträglichkeit verfügbar sind. Die häufig beworbenen Titanstimulations- oder genetische Tests gelten nur als „hinführende“ Diagnostik.
Wie kommen Titanpartikel ins Gewebe?
Als Quellen für Titanpartikel werden einerseits Abrieb beim Einbringen der Implantate oder Mikrobewegungen zwischen Implantat und Abutment angenommen. Weiterhin kann ein saures entzündliches Niveau Korrosion der chemisch inerten Implantatoberfläche bewirken. In diesem Fall sind Ursache und Wirkung nicht klar von einander abgrenzbar, so dass weitere Forschung erforderlich ist.
Zirkonoxid wohl nicht biokompatibler
Titanallergien sind sehr selten und eine eindeutige Diagnose Titanunverträglichkeit aus den genannten Gründen schwierig. Daher sollte erst nach sorgfältiger Anamnese und klinischer Befundung explantiert werden. Einteilige Keramikimplantate gelten inzwischen als klinisch bewährt. In Bezug auf zum Beispiel Entzündungs-Biomarker im Weichgewebe, Sondierungsblutung und weitere klinische Messwerte besteht aber nach einer Literaturauswertung von PD Dr. Paul Weigl (Frankfurt) möglicherweise kein Unterschied zu Titan [5-7].
Entscheidend könnte auch hier nach Auffassung verschiedener Referenten das individuelle Risikoprofil im Sinne einer Risiko-Stratifizierung sein [5]. Keramikimplantate sind daher nach Meinung der DGI-Leitlinienkommissionen und fast aller Kongressreferenten bei Verdacht auf materialbedingte Unverträglichkeit kein Ersatz für Titanimplantate. Sie seien vor allem indiziert, wenn Patienten vor einer primären Implantation aus persönlichen Gründen „weiße“ Implantate bevorzugen.
Bei Verdacht auf Materialunverträglichkeit sollte auch an Reaktionen auf Abutments und die implantatprothetische Suprakonstruktion gedacht werden. In Frage kommt laut dem neuen DGI-Präsidenten Prof. Dr. Florian Beuer zum Beispiel elektro-chemische Korrosion unter Beteiligung von Kobalt-Chrom-Legierungen. Vorteile gegenüber diesem Werkstoff hat Titan, weiterhin ist die CAD/CAM-Fertigung gegenüber Gussverfahren zu bevorzugen. Materialbezogen zeigte Beuer auf Basis der auch hier eingeschränkten Datenlage, dass zum Beispiel PMMA im Kontakt zu Weichgewebe überraschend biokompatibel ist [8]. Das gilt auch für Lithiumdisilikat, das sich möglicherweise sogar günstiger als Zirkonoxid verhält [9].
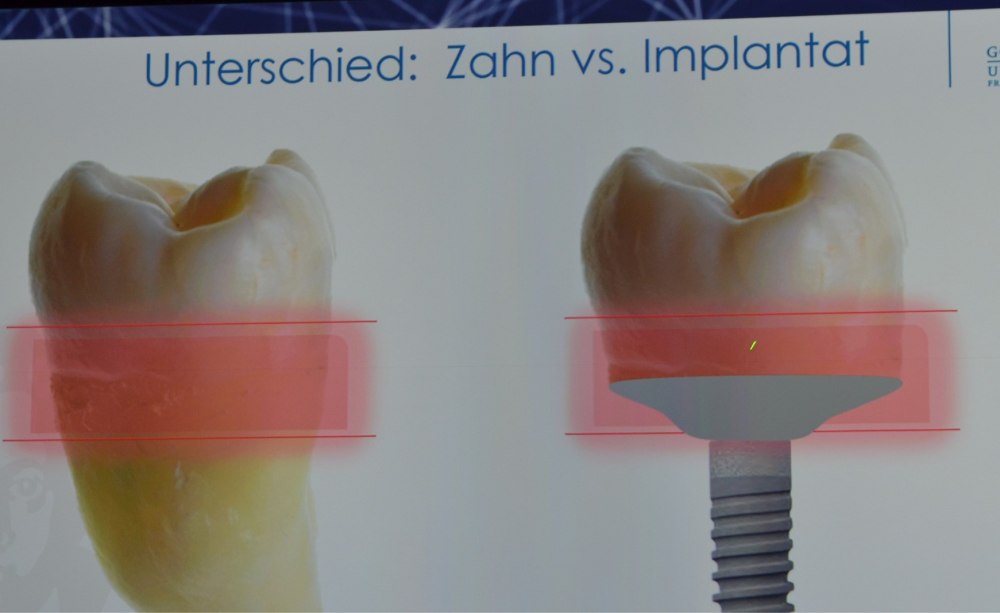
Der „transmukosale“ Bereich zwischen knöcherner Verankerung und Weichgewebsrand hat einen entscheidenden Einfluss auf die Implantatprognose (Präsentation PD Dr. Paul Weigl).
Ehrenmitgliedschaft und Karl-Ludwig-Ackermann-Medaille
Neues Ehrenmitglied der DGI ist der Kasseler MKG-Chirurg Prof. Dr. Dr. Hendrik Terheyden. Sein Kieler Kollege und DGZMK-Präsident Prof. Dr. Dr. Jörg Wiltfang hob hervor, dass Terheyden die wissenschaftliche Basis der oralen Implantologie entscheidend förderte, unter anderem mit den vier ersten Leitlinienprojekten der DGI im Jahr 2010.
Die neu eingeführte Dr. Karl-Ludwig Ackermann-Medaille erhielt Prof. Dr. Dr. Peter Tetsch (Münster) für sein herausragendes Lebenswerk. In seiner Laudatio betonte der ehemalige DGI-Präsident Prof. Dr. Dr. Volker Strunz Tetschs großen Beitrag dazu, dass die orale Implantologie aus dem ehemaligen „Rotlicht-Milieu“ zu einem anerkannten wissenschaftlichen Teilgebiet der Zahnmedizin wurde.

Ehrenmitglied Prof. Dr. Dr. Hendrik Terheyden (Mitte), mit Ehefrau Dr. Eva Ulrike Terheyden-Niemann und Kongress-Kopräsident Prof. Dr. Dr. Knut A. Grötz. Foto: DGI/Bostelmann
Gero-Implantologie und Kardiologie
Vor einer implantologischen Versorgung bei alten Patienten sollten Mundhygiene-Fähigkeit, soziale Aspekte und nicht zuletzt die orale Funktion untersucht werden. Zu dieser zählen laut PD Dr. Samir Abou-Ayash (Bern) Kaudruck, Zungendruck und Lippendruck, die Aufschluss über den Allgemeinzustand des Patienten erlauben. Weiterhin sollte der Immunstatus untersucht werden, der sich im Alter in Richtung chronische Entzündung entwickelt. Aus diesem Grund sei trotz größerer Plaque-Ansammlung nicht immer eine akute Entzündung festzustellen. Um einer Periimplantitis vorzubeugen, könnte eine Immunmodulation sinnvoll sein.
Wissenschaftlich evaluierte Daten, die eine geeignete Therapie-Entscheidung stützen könnten, stehen laut Abou-Ayash für Europa noch nicht zur Verfügung. Das aktuelle Konzept der Berner Universität sieht vor, möglichst kleine Implantate zu verwenden, die auf der Basis von 3-D-Diagnostik schablonengeführt eingesetzt werden. Die äußere Form von Totalprothesen wird dabei nach Möglichkeit nicht verändert, der „Unterbau“ aber an die Patientensituation angepasst.

Antibiotika-Prophylaxe nur für kardiale Hochrisiko-Patienten (Prof. Dr. Dr. Søren Jepsen und Prof. Dr. Stefan Frantz).
Ein weiteres durchgängiges Kongressthema waren systemische, mit einem Fokus auf Herz-Kreislauf-Erkrankungen. Für die Deutsche Gesellschaft für Parodontologie informierte Prof. Dr. Dr. Søren Jepsen (Bonn), dass zu Bakteriämien bei Periimplantitis wenig bekannt ist. Ein therapeutischer Effekt in Bezug auf Herz-Kreislauf-Erkrankungen ist auch bei Parodontitis schwierig nachzuweisen, aber plausibel und das wird auch von internistischen Kollegen so gesehen. Daher sollten Parodontitis-Patienten auf ein erhöhtes Risiko für kardiovaskuläre Erkrankungen hingewiesen werden. Parallel sollten Kardiologen und Hausärzte über diesen Zusammenhang aufklären und gegebenenfalls zum Oralarzt überweisen [10].
Aus kardiologischer Sicht betonte Prof. Dr. Stefan Frantz (Würzburg), dass Endokarditiden sehr selten auftreten. Entsprechend ist eine antibiotische Abschirmung nach aktuellen Empfehlungen nur bei Hochrisikopatienten indiziert, das sind solche mit Klappenprothesen, nach überstandener Endokarditis oder mit angeborenem Herzfehler [11]. Werden eine Bakteriämie und Entzündungsmarker nachgewiesen, kann eine Parodontitis-Therapie angezeigt sein. Das gilt ebenso vor Herzklappen-Operationen. Professor Jepsen ergänzte, dass wegen der systemischen Belastung bei Risikopatienten die Initialtherapie nicht in einer Sitzung vorgenommen werden sollte.
„Wir können nicht mehr ohne einander“
Mit zirka 750 angemeldeten Zuhörern der Fachvorträge und zusätzlich 450 Online-Teilnehmern war der DGI-Kongress wieder einmal gut besucht. Auch fachlich befand sich der DGI-Kongress 2021 auf dem gewohnten, sehr hohen Niveau. Zwar waren mit einer Internistin und einem Kardiologen nur zwei Referenten aus der „extraoralen“ Medizin vertreten, doch gab es eine ganze Reihe systemisch orientierter Vorträge von Zahnärzten und MKG-Chirurgen. Dass auch die oralen Teilgebiete immer enger zusammenrücken, brachte der Parodontologe Prof. Dr. Henrik Dommisch auf den Punkt: „Wir können nicht mehr ohne einander.“
In diesem Zusammenhang dürfen wir auf einen für 2023 angekündigten Workshop der European Federation of Periodontology gespannt sein. Dort könnte die EFP nach Einschätzung von Prof. Dr. Moritz Kebschull für einen Teil der Parodontitis-Patienten vor Implantationen warnen. Das Periimplantitis-Risiko ist bei diesen nach einer aktuellen Metaanalyse um den Faktor 3,3 erhöht (Risk-Ratio) [12]. Neben dem Immunstatus sind weitere Risikofaktoren wie Rauchen oder systemische Erkrankungen wie Diabetes zu beachten. Ob in näherer Zukunft ausreichend Daten für eine systemisch-immunologische, genetische oder mikrobiologische Risiko-Einschätzung von Patienten vorliegen werden, bleibt abzuwarten.
Die DGI hat sich kurzfristig entschlossen, dass die Mediathek mit den Präsentationen und Diskussionen noch bis zum 14. Januar gebucht werden kann. Die Kongress-Website ist also weiterhin geöffnet, hier geht zum Buchungsfenster.
Dr. Jan H. Koch, Freising
Hinweis: Teile der in Wiesbaden umfangreich präsentierten praktischen Inhalte werden in den kommenden Ausgaben des neuen Magazins dzw orale implantologie (oi) abgehandelt.

Das Team der DGI-Nachwuchsorganisation Nexte Generation: Die jungen Mediziner waren erstmals von Beginn in das inhaltliche Kongress-Konzept eingebunden und stellten mehrere Referenten.
Literatur
[1] Kunrath MF, Muradás TC, Penha N, Campos MM. Innovative surfaces and alloys for dental implants: What about biointerface-safety concerns? Dental Materials 2021;37:1447-1462.
[2] Albrektsson T, Buser D, Chen ST, Cochran D, DeBruyn H, Jemt T, et al. Statements from the Estepona Consensus Meeting on Peri-implantitis, February 2–4, 2012. Clin Implant Dent Relat Res 2012;14:781-782.
[3] Nelson K, Hesse B, Addison O, Morrell AP, Gross C, Lagrange A, et al. Distribution and Chemical Speciation of Exogenous Micro- and Nanoparticles in Inflamed Soft Tissue Adjacent to Titanium and Ceramic Dental Implants. Anal Chem 2020;92:14432-14443.
[4] Bressan E, Ferroni L, Gardin C, Bellin G, Sbricoli L, Sivolella S, et al. Metal Nanoparticles Released from Dental Implant Surfaces: Potential Contribution to Chronic Inflammation and Peri-Implant Bone Loss. Materials (Basel) 2019; 12(12).
[5] Cionca N, Hashim D, Cancela J, Giannopoulou C, Mombelli A. Pro-inflammatory cytokines at zirconia implants and teeth. A cross-sectional assessment. Clin Oral Investig 2016;20:2285-2291.
[6] Bienz SP, Hilbe M, Husler J, Thoma DS, Hammerle CHF, Jung RE. Clinical and histological comparison of the soft tissue morphology between zirconia and titanium dental implants under healthy and experimental mucositis conditions-A randomized controlled clinical trial. J Clin Periodontol 2021;48:721-733.
[7] Desch A, Freifrau von Maltzahn N, Stumpp N, Dalton M, Yang I, Stiesch M. Biofilm formation on zirconia and titanium over time-An in vivo model study. Clin Oral Implants Res 2020;31:865-880.
[8] Shim JS, Kim HC, Park SI, Yun HJ, Ryu JJ. Comparison of Various Implant Provisional Resin Materials for Cytotoxicity and Attachment to Human Gingival Fibroblasts. Int J Oral Maxillofac Implants 2019;34:390-396.
[9] Jung S, Moser MM, Kleinheinz J, Happe A. Biocompatibility of Lithium Disilicate and Zirconium Oxide Ceramics with Different Surface Topographies for Dental Implant Abutments. Int J Mol Sci 2021;22.
[10] Sanz M, Marco Del Castillo A, Jepsen S, Gonzalez-Juanatey JR, D’Aiuto F, Bouchard P, et al. Periodontitis and cardiovascular diseases: Consensus report. J Clin Periodontol 2020;47:268-288.
[11] DGMKG, DGZMK. S2k-Leitlinie (Langversion): Zahnsanierung vor Herzklappenersatz. AWMF-Registernummer: 007-096, Stand: April 2017. Gültig bis: April 2022.
[12] Carra MC, Rangé H, Swerts PJ, Tuand K, Vandamme K, Bouchard P. Effectiveness of implant-supported fixed partial denture in patients with history of periodontitis: A systematic review and meta-analysis. J Clin Periodontol. online 20211114.