Zeitschriftenbeiträge zu computergestützter Implantologie tauchten in der PubMed-Datenbank erstmals vor fast 25 Jahren auf [1]. Seitdem ist vieles technisch eleganter und patientenfreundlicher geworden. Die meisten Zahnärzte implantieren bis heute dennoch ohne Computer. Warum das nicht ideal ist und wohin die Reise mit neuer Visualisierungstechnik gehen könnte, lesen Sie hier.
Knapp und klar
• DVT-Diagnostik sollte dem ALADA-Prinzip entsprechen (As Low As Diagnostically Advisable).
• Höhere Kosten für geführte Implantationen werden fallabhängig durch erhöhte Sicherheit und vermiedene Augmentationen ausgeglichen.
• Da mehrere techniksensitive Schritte notwendig sind, gilt weiterhin ein Sicherheitsabstand von mindestens 2 mm zu gefährdeten Strukturen.
• Stand der Technik ist ein Abgleichen gescannter intraoraler Oberflächen mit den Dicom-Daten.
• Je nach Restbezahnung können Röntgenschablonen erforderlich sein.
• Durch die Fusion von intra-, extraoralen und Funktionsdaten kann die Planung weiter verbessert werden.
Wann 3-D-Diagnostik mit DVT?
3-D-Diagnostik mit DVT wird zum Beispiel für anatomische Besonderheiten, pathologische Befunde oder „spezielle chirurgische und prothetische Therapiekonzepte wie Sofortversorgung, navigationsgestützte Implantologie und komplexe interdisziplinäre Therapiekonzepte“ eingesetzt [2, 3]. Damit ist der Rahmen recht weit gesteckt, einschränkend wirkt vor allem das Prinzip der Strahlenhygiene. Nach dem ALADA-Prinzip (As Low As Diagnostically Advisable) sollte DVT nur zum Einsatz kommen, wenn notwendige diagnostische Informationen mit geringerer Strahlendosis nicht zu bekommen sind [4]. Oder wenn der Patient nicht altersbedingt oder wegen früherer Belastung so weit wie möglich geschont werden sollte. Positiv wirkt sich aus, dass für die Planung von Implantatpositionen heute in der Regel eine relativ geringe Auflösung ausreicht.
Inwieweit hilft "3-D-Implantologie" dem Patienten?
Doch wer dreidimensional diagnostiziert, muss nicht notwendigerweise computergestützt planen. Und wer computergestützt plant, muss nicht geführt aufbereiten und implantieren. Grund sind häufig die Kosten, die bereits bei der Röntgenaufnahme eine Rolle spielen und bei softwarebasierter Planung und Herstellung einer Bohrschablone bedeutsamer werden. Andererseits ist die Frage relevant, inwieweit „3-D-Implantologie“ Augmentationen [5], chirurgische Komplikationen oder prothetische Misserfolge vermeiden hilft und damit Patienten erheblich nutzt.
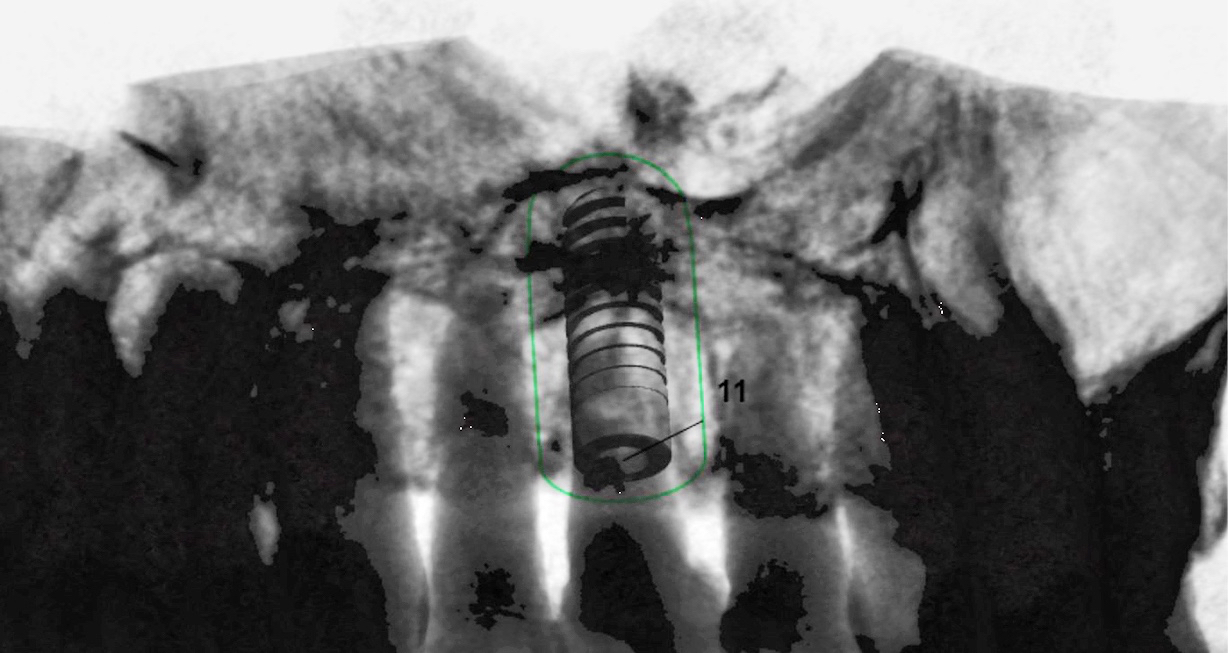
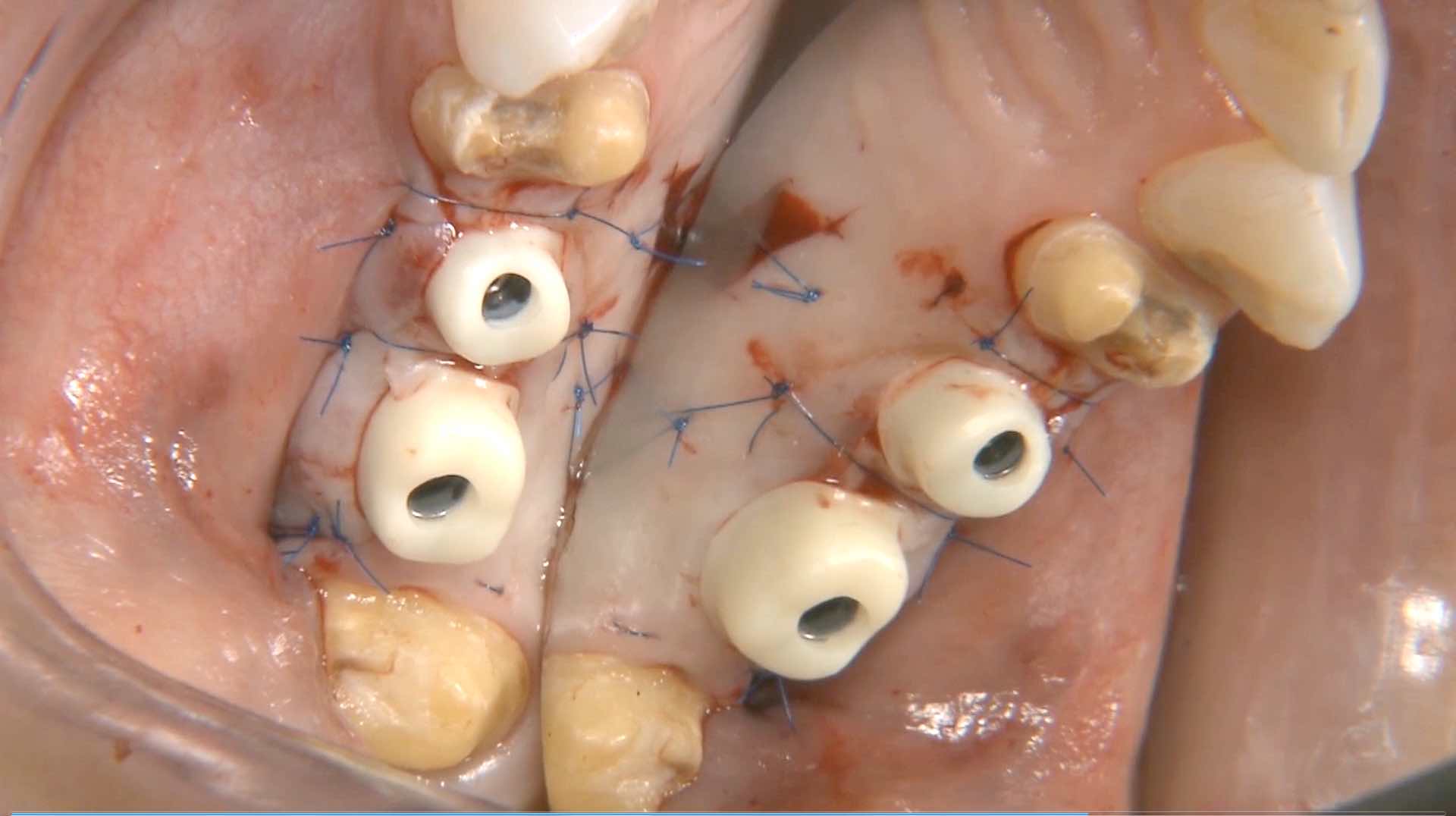
Für wenig belastbare, zum Beispiel geriatrische Patienten oder solche mit engem Zeitbudget, lässt sich schließlich durch computergestützte Implantologie die Zahl der Sitzungen, aber auch die der chirurgischen Eingriffe, reduzieren (Abb. 1 und 2) [6, 7]. Mit zusätzlich genutzter lappenloser Operationstechnik können zudem zahnlose Kiefer tendenziell schonender versorgt werden als mit großflächiger Aufklappung [8]. Dies spielt besonders bei Patienten mit Vorerkrankungen oder unter gerinnungshemmender Medikation eine Rolle [9].
Genauigkeit und DVT-Technik
Ziel computergestützter Verfahren ist unter anderem eine bessere Genauigkeit des chirurgischen und damit auch des prothetischen Ergebnisses. Hier gibt es nach wie vor Probleme, die unter anderem auf dem techniksensitiven Verfahren beruhen. Im neuesten Konsenspapier des International Team for Implantology (ITI) wird deshalb ein periimplantärer Sicherheitsabstand von mindestens 2 mm zu gefährdeten Strukturen empfohlen [8]. Im ungünstigen Fall kann sogar dieser Wert zu gering sein, sodass bei jedem Schritt höchste Sorgfalt geboten ist [10].
Eine höhere DVT-Auflösung führt nicht zu genauer geplanten Implantatdimensionen und -positionen. Daher empfehlen die Experten, am DVT eine Voxelgröße von 0,3 bis 0,4 mm3 einzustellen. Weiterhin sollte das kleinstmögliche Aufnahmevolumen unter Nutzung gerätespezifischer Rotationsmöglichkeiten gewählt werden. Zu beachten ist, dass sich Geräte in Bezug auf Strahlendosis und erreichbare Genauigkeit erheblich unterscheiden können [11, 12]. Weiterhin ist auf ein fachgerechtes Patientenmanagement und eine geeignete Aufnahmetechnik zu achten [13].
Datengewinnung und Bohrschablonen
Für teil- wie für unbezahnte Fälle wird im ITI-Konsens ein Abgleich (Matching) radiologischer DICOM- mit Oberflächendaten empfohlen [8]. Letztere werden über intraorale oder Laborscans von Modellen (bei ausreichender Restbezahnung, mit oder ohne Set-up), über speziell angefertigte Röntgenschablonen oder vorhandene Prothesen gewonnen [14]. Die Bohrschablonen werden dann auf Basis der gematchten Daten konstruiert (Abb. 3 bis 5). Dies führt zu genaueren Implantatpositionen als bei laborgestützter Herstellung mit physischer Übertragung („Giraffe“) [15]. Zudem lässt sich auf diese Weise die Weichgewebsdicke recht genau einschätzen, sodass Abutments und Prothetik viel besser planbar sind als auf der Basis radiologischer Daten [6].
Die softwaregestützte Berechnung der Schablone – und damit der Bohrhülsen – hat neben der Präzision einen weiteren sehr wichtigen Vorteil: Eine beim Scan unpräzise sitzende Röntgenschablone führt nur zu einer Fehlpassung der Schablone, nicht zu falsch präparierten Implantatlagern wie bei physischer Übertragung [7]. Herstellungswege für Bohr- und – wenn notwendig – Röntgenschablonen sind vielfältig und vom Workflow zwischen Praxis und Labor oder Fräszentrum und vom Produktsystem abhängig. Auch bei letzteren scheint es herstellerabhängige Qualitätsunterschiede zu geben [16].
Was tun bei Schlotterkamm?
Für genaue Ergebnisse ist eine ganze Reihe prozesstechnischer Details zu beachten. So sollten bei DVT-Aufnahmen für korrekte Darstellung der bukkalen Alveolarmukosa die Wangen mit Watterollen ferngehalten werden [17]. Um Artefakte durch metallische Restaurationen so weit wie möglich zu vermeiden, werden die Zahnreihen zum Beispiel mit Holzspateln gesperrt. Bei Freiendsituationen oder für den Fall einer Aufklappung empfiehlt es sich, Bohrschablonen auf der Tuberschleimhaut abzustützen (kombinierte Zahn- und Weichgewebslagerung). Bei zahnlosen Patienten mit Weichgewebshyperplasie oder Schlotterkamm kann sogar eine Knochenlagerung erforderlich sein [14]. Um eine hohe Genauigkeit zu erreichen, sind zudem einige hardwarespezifische Parameter zu beachten [10] (vgl. Abb. 2):
• Länge der Bohrhülsen
• Abstand zwischen Knochenbohrer und Bohrhülseninnenseite
• Implantatlänge
• Distanz zwischen Bohrhülsenoberkante und Implantatschulter
Datenbrillen und gedrucktes Gewebe
Als Alternative zu „statischen“ geführten Aufbereitungssystemen wurden in jüngster Zeit „dynamische“ weiterentwickelt (Abb. 6) [19]. Damit lassen sich bei unerwarteten Knochendefiziten Implantatachsen intraoperativ anpassen, ohne dass eine erneute Planung notwendig ist [20]. Ein weiterer Schritt könnte die Verwendung von Datenbrillen sein, mit denen ein Blickwechsel vom Patienten entfällt und die bereits für das intraorale Scannen erhältlich sind (eCc). Prinzip dieser „augmentierten Realität“ (AR) ist – ähnlich wie beim Entwerfen von animierten Filmfiguren auf der Basis menschlicher Mimik – eine Überlagerung der realen Situation mit virtuell erstellten Bildern und Videos (Abb. 7). Dreidimensionale Techniken einschließlich Gewebedruck werden bisher vor allem epithetisch, kieferchirurgisch und kieferorthopädisch-chirurgisch genutzt, könnten sich aber auch in der zahnärztlichen Prothetik etablieren.
Fazit
Zahnärzte, die computergestützt implantieren wollen, sollten ausreichende Erfahrung und ein umfassendes Training absolviert haben [8]. Bis heute fehlen Studien, die für computergestützte Verfahren bessere Operationsergebnisse und eine geringere Anzahl von Komplikationen zeigen [3, 8]. Dies ist jedoch angesichts der hohen Fallzahl vergleichbarer Patientenfälle schwierig, die für eine geforderte Randomisierung notwendig wären. Nach übereinstimmender Expertenmeinung bereichert die Technik die implantatprothetischen Möglichkeiten. Entwicklungen wie dynamische Navigation, Visualisierungstechniken und deren Transfer in Knochenaugmentate, Gewebeersatz oder – auch an die extraorale Situation – angepasste Implantatprothetik lassen zudem für die Zukunft noch einiges erwarten.
Dr. Jan H. Koch, Freising
Hinweis: Dieser Beitrag kann nicht die klinische Einschätzung des Lesers ersetzen. Er soll lediglich – auf der Basis aktueller Literatur und/oder von Expertenempfehlungen – die eigenverantwortliche Entscheidungsfindung unterstützen.
Das Literaturverzeichnis kann angefordert werden unter leserservice@dzw.de