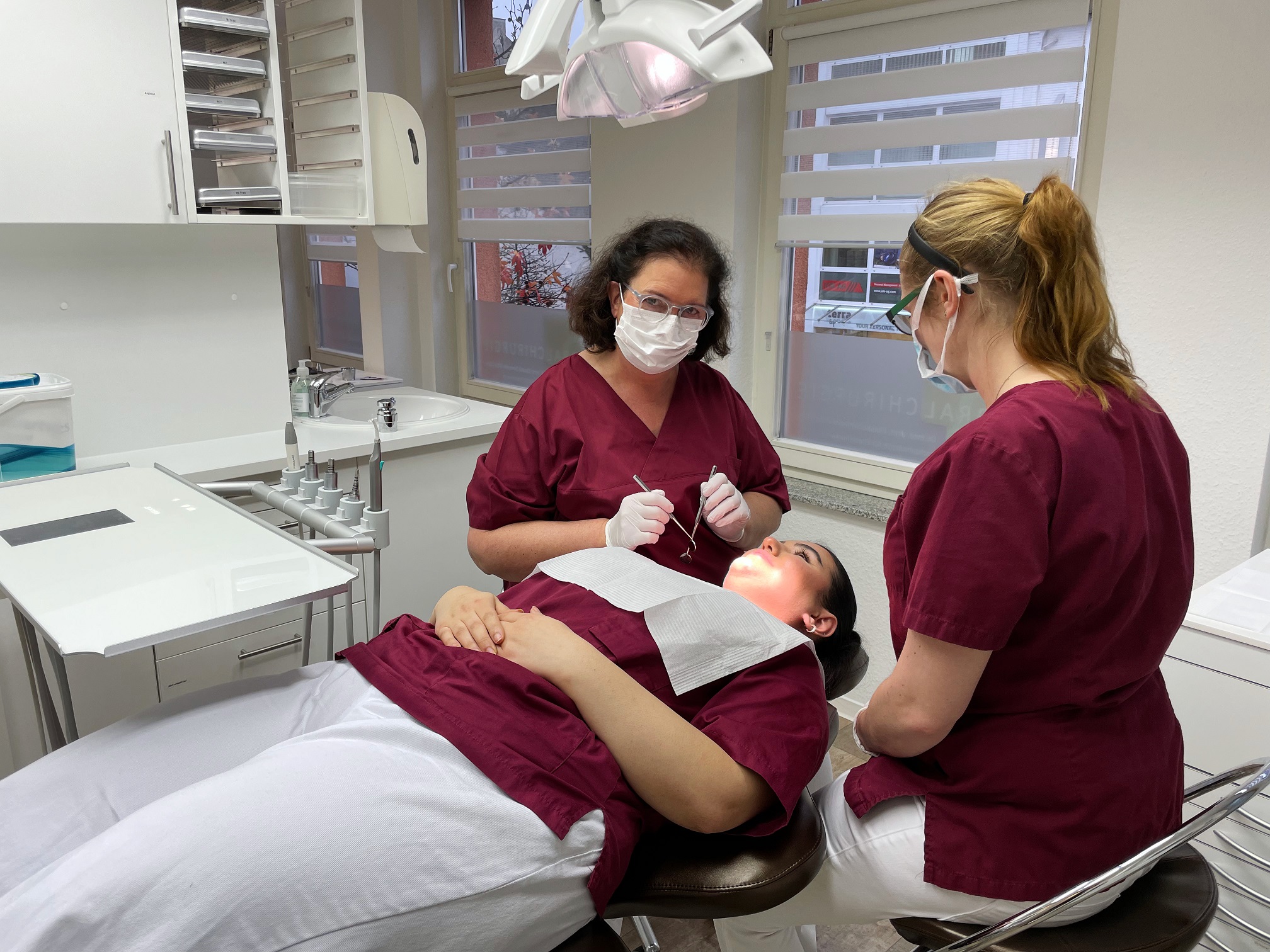
Patientenorientierte Absprachen zwischen Zahnarzt und Prophylaxekraft schaffen einen Qualitätsanstieg und vertrauensvolle Patientenbindungen in der Implantatnachsorge.
In den vergangenen Jahrzehnten hat sich die Zahl der inserierten Implantate in Deutschland stetig erhöht, das Spektrum der prothetischen Versorgungsmöglichkeiten ist gewachsen. Der Patient gewinnt dadurch an Komfort und Lebensqualität. Darum sollte er, für einen möglichst lebenslangen Erhalt seiner Implantate, begleitet werden.
Bakterielle Biofilme wurden in zahlreichen präklinischen und klinischen Studien als der ätiologische Faktor für die Entstehung einer periimplantären Mukositis herausgestellt [1]. Es wird angenommen, dass eine periimplantäre Mukositis einer Periimplantitis vorausgeht, insbesondere wenn keine regelmäßige Plaquekontrolle durchgeführt wird. Ebenso gibt es Hinweise, dass Patienten, die keine regelmäßige Nachsorge erhalten, ein höheres Risiko für Periimplantitis haben [2]. Der Verlauf einer Periimplantitis geht mit einem Verlust des Stützknochens einher, folglich kann es zum Implantatverlust kommen. Die Progressionsrate kann, verglichen mit einer Parodontitis, erhöht sein.
Immer mehr Patienten mit Bedarf einer intensiven Betreuung
Demnach hat das Vermeiden einer Biofilmakkumulation besondere Bedeutung. Eine präventionsorientierte Praxis kann den Patienten maßgeblich bei der anzustrebenden Implantatgesundheit unterstützen. Durch den deutlich vermehrten Einsatz von Implantaten wird es auch einen Zuwachs von periimplantären Erkrankungen geben, für die zahnärztliche Praxis bedeutet das einen Anstieg von Patienten mit Bedarf einer intensiven Betreuung.
Risiken bestimmen die Frequenz der UIT
Die Häufigkeit der notwendigen Implantatnachsorge, auch unterstützende Implantatherapie (UIT) genannt, wird durch die beeinflussenden Risiken bestimmt. Die Entstehung von periimplantären Erkrankungen kann sowohl durch lokale (das heißt das Implantat betreffende) als auch systemische (das heißt den Patienten betreffende) Risikofaktoren begünstigt werden [3].
Folgende allgemeinanamnestische Punkte beeinflussen die Intensität der Betreuung und Therapieplanung des Patienten:
• schlecht eingestellter Diabetes mellitus
• Rauchen
• Medikamente (antiresorptive Therapie mit Bisphosphonaten oder Denosumab, Immunsuppressiva)
• vorausgegangene Bestrahlungs- oder Chemotherapie
Lokale Risikofaktoren können folgende sein:
• parodontale Vorerkrankungen (residuale Taschen, nicht behandelte Parodontitis)
• Fehlen einer keratinisierten Gingiva/Weichgewebsdefekte
• insuffiziente Mundhygiene
• biologisch und technisch assoziierte Risikokomponenten
• klinische Entzündungszeichen an der Mukosa/Vorhandensein einer periimplantären Mukositis
• verminderter Speichelfluss/Xerostomie
Geführte Anamneseerhebung
Risikofaktoren sollten schon vor der Implantation erkannt werden und aufgrund von möglichen Änderungen bei jeder Nachsorge neu aufgenommen werden. Eine geführte Anamneseerhebung ist dabei ein großer Vorteil. Ein gezielt geführtes Gespräch mit dem Patienten kann helfen, systemische Risiken sicher und korrekt zu erfassen und analysieren. Der Zahnarzt kann dabei maßgeblich von seiner Zahnmedizinischen Prophylaxe-, Fachassistentin oder Dentalhygienikerin unterstützt werden.
Das Praxisteam kostet die anamnestische Befragung Zeit, gleichzeitig macht sie auf den Patienten einen aufmerksamen und kompetenten Eindruck. Der Patient sollte den Zusammenhang zwischen dem Entstehen einer Periimplantitis und seinen persönlichen ätiologischen Risiken kennen. Der vorab erbrachte zeitliche Aufwand zahlt sich für die Praxis in allen Nachfolgesitzungen aus. Implantatgesundheit ist eng an ein Präventionskonzept gekoppelt, ein gut aufgeklärter Patient wird regelmäßig die UIT wahrnehmen.
Eine strukturierte UIT beinhaltet folgende Punkte:
• Aufnahme/Aktualisieren der dentalen und allgemeinen Anamnese
• intraoraler Befund (unter anderem zur Überprüfung von risikoassoziierten biologischen oder technischen Komponenten)
• schonendes Sondiertiefenmessen und Blutung auf Sondierung aufnehmen
• Aufnahme eines Mundhygienebefundes
• Mundhygieneinstruktion und Remotivationsgespräch mit dem Patienten
• Eine professionelle Zahnreinigung und submuköse Instrumentierung
• Festlegung des UIT-Intervalls, bestimmt durch das individuelle Risikoprofil
Das Biofilmmanagment nimmt bei der UIT einen hohen Stellenwert ein. Mit einer klaren Leistungsverteilung im Team kann der Zahnarzt Bestandteile der Nachsorge an seine hochqualifizierte Prophylaxefachkraft delegieren. Für den Zahnmediziner ist es Zeitersparnis, für die Praxis ein qualitativer und wirtschaftlicher Gewinn, und für den Patienten schafft es eine intensive Betreuung.
Engmaschige Kontrolle bei Blutung auf Sondierung
Periimplantäre Gesundheit ist durch das Fehlen von Entzündungszeichen charakterisiert. Die periimplantäre Mukositis zeichnet sich unter anderem durch eine Blutung auf Sondieren (BAS; auch BOP) aus und geht einer Periimplantitis voraus. Ist eine Blutung auf Sondierung festzustellen, gilt es, diese engmaschig zu kontrollieren
Taschentiefe regelmäßig aufnehmen
Für die periimplantäre Mukositis konnte vornehmlich das Rauchen als unabhängiger systemischer Risikofaktor identifiziert werden [4]. Ebenso wird die Entstehung der Periimplantitis insbesondere durch parodontale Vorerkrankungen und das Rauchen [5] begünstigt. Sind im Restgebiss noch residuale Taschen vorhanden, gilt dies als Risiko für eine periimplantäre Infektion. In der UIT sollten regelmäßig Taschensondierungstiefen aufgenommen werden, um eine parodontale Stabilität zu überprüfen oder erneut eine systematische Parodontaltherapie zu intendieren.
Risikofaktoren Speichelfluss oder Xerostomie
Ein weiteres Risiko kann ein verminderter Speichelfluss oder Xerostomie sein. Der Speichel hat protektive Eigenschaften, durch eine geringere Speichelfließrate kann es zu einer erhöhten Plaquebildungsrate kommen.
Auch das Vorhandensein beziehungsweise ein schlecht eingestellter Diabetes mellitus gilt als ätiologischer Risikofaktor. Im Zusammenhang mit Parodontitis ist ein bidirektionaler Zusammenhang sichergestellt.
Lokale und systemische Risikofaktoren werden als Gesamtpaket betrachtet und geben einen starken Hinweis auf das Intervall der UIT. Zahnarzt und Prophylaxefachkraft sollten in gemeinsamer Absprache die Nachsorgefrequenz festlegen. Gemeinsam sorgen sie für eine hervorragende Patientenbindung und effiziente Patientenführung.
Nachsorge-Intervall individuell an Patienten anpassen
Mögliche Empfehlungen können zwischen drei bis zwölf Monaten liegen, jedoch fehlen evidente Daten für die Festlegung des Intervalls. Bei fehlenden Risikofaktoren und guter Mundhygiene könnte eine Zeitspanne von sechs bis zwölf Monaten indiziert sein. Sobald Risikofaktoren hinzukommen, kann die Nachsorgefrequenz auf drei bis vier Monate erhöht werden. Das Intervall sollte individuell an jeden Patienten angepasst werden.
Christin Damann

Christin Damann ist Dentalhygienikerin, seit 2016 angestellte Fortbildungsreferentin der Zahnärztekammer Westfalen-Lippe und DH in der zahnärztlichen Praxis Dres. Leineweber, Bocholt
Literatur
S3-Leitlinie: Die Behandlung periimplantärer Infektionen an Zahnimplantaten AWMF-Registernummer 083-0237
Oralprophylaxe & Kinderzahnheilkunde 40 (2018) 3
1: Renvert &Polyzois 2014
2: Berglund et al. Journal of Clinical Periodontology 2018
3: Schwarz & Becker 2015
4: Renvert & Polyzois 2014
5: Heitz-Mayfield 2008