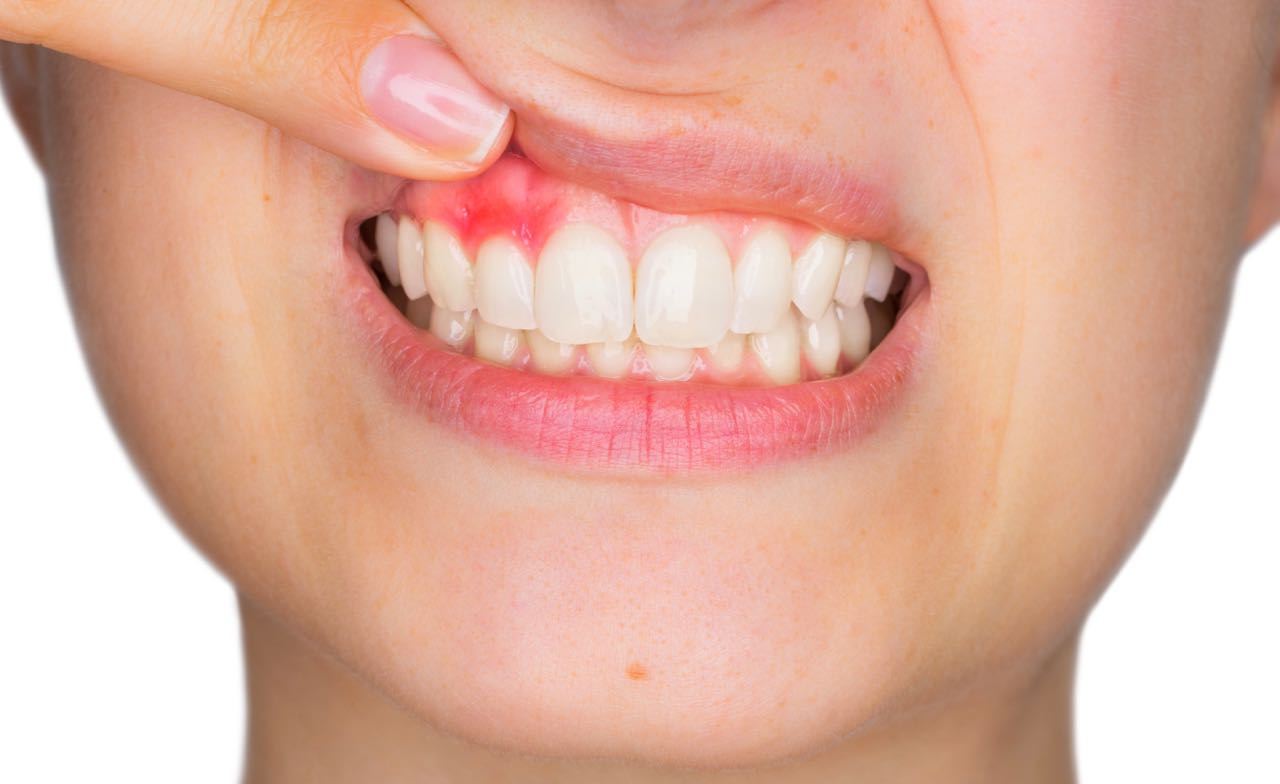
Bei Patienten mit florider Parodontitis sind bakterielle Antigene und zirkulierende Biomarker im Sulkusfluid und in geringerer Konzentration auch im Speichel nachweisbar.
Bei Patienten mit florider Parodontitis sind bakterielle Antigene und zirkulierende Biomarker im Sulkusfluid und in geringerer Konzentration auch im Speichel nachweisbar. Untersuchungen gingivaler und parodontaler Läsionen hinsichtlich der Entzündungsparameter und der mikrobiellen Aktivität geben wertvolle Aufschlüsse über die aktuelle Krankheitssituation und bedingt auch über eine mögliche Progression der Entzündung. Sie ermöglichen Ansätze für eine individuell abgestimmte effektive Therapie.
Parodontitis wird heute als multifaktorielle Erkrankung mit langfristiger Destabilisierung des oralen Mikrobioms gesehen. Durch die Artenverarmung der ursprünglichen oralen Flora und einem Überhandnehmen potenziell pathogener Mikroorganismen kommt es zur Etablierung von subgingivalen Biofilmen. In diesen ist aufgrund komplexer bakterieller Interaktionen sowohl die Virulenz als auch die Resistenz der Erreger gegen Antibiotika und lokale Plaquehemmer gegenüber frei in der Mundhöhle lebenden Mikroorganismen um Zehnerpotenzen erhöht.
Während noch vor Kurzem die meist anaeroben oder fakultativ anaeroben Leitkeime im Brennpunkt des Interesses standen, weiß man heute, dass neben diesen durchaus aggressiven Pathogenen auch zahlreiche andere, zum Teil atypische und nicht zur eigentlichen Mundflora gehörige Bakterienspezies die entzündlichen Prozesse und den Gewebeabbau vorantreiben. Sowohl die Komposition der parodontal-pathogene Mikroflora als auch die Reaktion der oralen Gewebe und der lokalen und systemischen Abwehr auf die Entzündungsreize zeigen große individuelle Variabilität. Systemische Vor- und Grunderkrankungen, genetische Faktoren und Lebensstil modifizieren Ausmaß und Verlauf chronischer Parodontopathien. All diese Parameter machen ein ganzheitliches Herangehen und eine möglichst umfassende Abklärung des Krankheitsgeschehens erforderlich.
Keimanalyse und Wirtsreaktion als diagnostisches Instrument
Für mikrobiologische Untersuchungen des Sulkusfluids stehen sowohl Kulturtechniken mit umfassender Keimanalyse und der Möglichkeit der Erstellung von Antibiogrammen, als auch molekularbiologische Methoden, die eine Bestimmung und Semiquantifizierung bestimmter Leitkeime ermöglichen, zur Verfügung. Letztere Tests umfassen vor allem die pigmentierten Anaerobier wie Prevotella intermedia, Porphyromonas gingivalis, Tannerella forsythia, Treponema denticola und den mit aggressiver Parodontitis assoziierten Aggregatibacter actinomycetemcomitans. Einteilungen dieser Keime hinsichtlich ihrer Virulenz und Bedeutung für die parodontale Entzündung in farbcodierte Komplexe ist zwar prinzipiell hilfreich, kann aber heute unter Einbeziehung unseres Wissens über die komplexe Struktur des oralen Mikrobioms nur noch als Teilaspekt bei der Diagnose angesehen werden. Sämtliche mikrobiologische Analysen sind in erster Linie eine Darstellung des aktuellen Zustandsbilds. Biologische Systeme unterliegen immer einer gewissen Variabilität. So kommt es auch in der oralen Biozönose durch exo- und endogene Einflüsse zu oft gravierenden Veränderungen, die eine regelmäßige Neubeurteilung und Kontrolle der mikrobiellen Situation erfordern.
Wie schon aus dem heterogenen Bild der parodontalen Erkrankungen ersichtlich, gibt es keine einheitlichen Biomarker. Quellen für Biomarker sind einerseits die subgingivalen Keime und ihre Stoffwechselprodukte, andererseits die Immunprodukte und Entzündungsmediatoren der Wirtsantwort. Aus den Entzündungszellen werden hydrolytische und proteolytische Enzyme freigesetzt, zudem entstehen Abbauprodukte der destruierten Gewebe.
Biomarker liefern Informationen über die aktuelle Krankheitsaktivität
Ein gängiger Test zur Bestimmung der Krankheits- und Entzündungsaktivität ist der BANA- Test. Dabei wird die aktuelle proteolytische Aktivität bestimmter anaerober Bakterien (im Wesentlichen: T.forsythia, T. denticola und P. gingivalis) bestimmt. Durch den enzymatischen Abbau von N-benzoyl-dl- Arginin entsteht der übelriechende Fötor ex orae. Wenn die betreffenden Keime und ihre Stoffwechselprodukte im Speichel vorhanden sind, kommt es zu einem Farbumschlag. Der Test hat in erster Linie eine patientenmotivierende Funktion. Nach Therapie und Einhaltung entsprechender Mundhygiene kann so ein unmittelbares Erfolgserlebnis vermittelt werden. Der diagnostische Wert ist eher gering, da schon am Mundgeruch und am klinischen und röntgenologischen Zustand des Zahnhalteapparats auf ein florides Krankheitsgeschehen geschlossen werden kann.
Andere Tests nehmen vorwiegend Bezug auf die Wirtsreaktion. So werden durch die Reize bakterieller Antigene Metalloproteinasen (MMP) in die Sulkusflüssigkeit und in den Speichel freigesetzt. Besonders MMP8 (Kollagenase-2) und MMP9 (Gelatinase-B) sind an der Degradierung des parodontalen Bindegewebes und der extrazellulären Matrixproteine des Zahnhalteapparats wesentlich beteiligt. Tests auf Metalloproteinasen können daher zusätzliche Information über die enzymatische Aktivität der Gewebedestruktion geben. Speichel- und Sulkusspiegel von MMP8 und MMP9 sind bei Parodontitispatienten gegenüber oral Gesunden deutlich erhöht, während die Metalloproteinase MMP-2 bei florider Entzündung erniedrigt ist. Die Speichelspiegel korrelieren mit dem gingivalen Blutungsindex und der „probing depth“. Allerdings ist eine mikroskopische Analyse des Sulkusfluids zur Bestimmung der Anteile der lytischen Granulozyten und der Makrophagen fast ebenso aufschlussreich. Seltener eingesetzte Tests mittels ELISA können den Level von Interleukinen (IL1a, Il1ß) quantifizieren, welcher in Zusammenhang mit der Osteoklastenaktivität und damit mit der Kieferknochenresorption steht.
Aspartat-Aminotransferase, Lactatdehydrogenase und alkalische Phosphatase sind Biomarker für Zerstörung und Nekrose von Geweben und korrelieren mit der parodontalen Taschentiefe des Patienten. Allerdings ist aus dem Speichel- und Sulkusfluidspiegel dieser Enzyme kein Rückschluss auf die Progression der Erkrankung möglich. Die Marker differenzieren nicht zwischen progredienten und zwar entzündeten, aber stabilen Läsionen.
Auch eine Reihe anderer Biomarker wie Kalzium oder Peroxidase sind bei Parodontitis im Sulkus erhöht, ebenso besteht eine positive Korrelation zwischen Speichel IgA und dem Ausmaß der Entzündung.
Zukunftsperspektive „Speichelproteom“
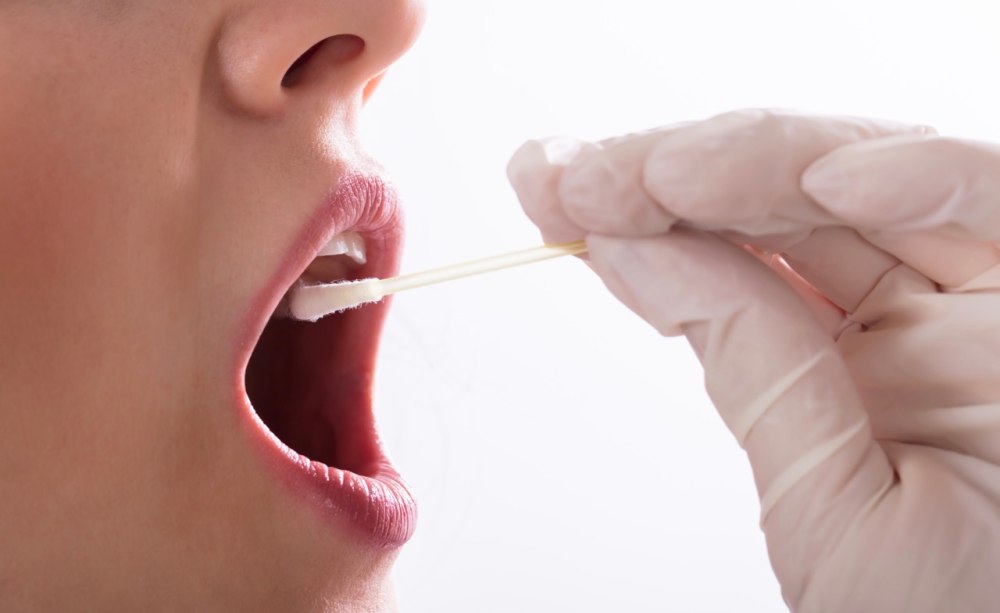
Die Speichelanalyse als Möglichkeit einer nicht-invasiven Diagnostik gingivaler und parodontaler Erkrankungen bietet einige interessante Ansätze, die derzeit Gegenstand zahlreicher Untersuchungen sind. Parallel mit der Erforschung des oralen Mikrobioms gilt das Interesse auch dem Speichel-Proteom. Darunter versteht man die Gesamtheit der Speicheleiweiße, welche ständigen Veränderungen durch Stoffwechsel, Synthese und Zelltod (Apoptose) unterworfen ist. Bestimmte Krankheitsmuster beeinflussen wesentlich das Gleichgewicht des Proteoms und verschieben dessen Anteile in charakteristischer Art und Weise. Bisher wurden mehr als 1.000 Speichelproteine identifiziert. Weitere Forschungsergebnisse könnten in Zukunft wesentlich zur Diagnose oraler Krankheiten beitragen.