Im ersten Teil des Beitrags zu "Fusobacterium nucleatum – der unterschätzte Keim" von DDr. Christa Eder geht es um das Stäbchenbakterium als Wegbereiter und Vermittler oraler Entzündungungen.
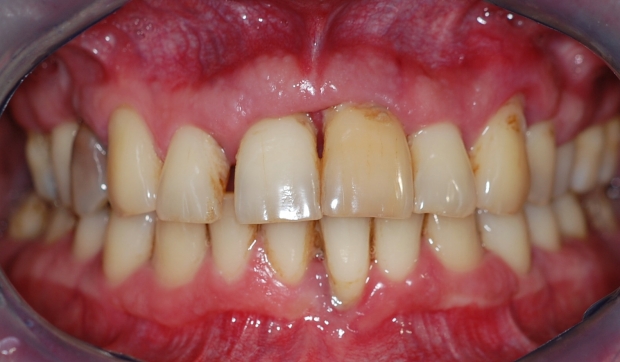
Gingivitis und Parodontitis werden durch Bakterien der subgingivalen Mikroflora ausgelöst und aufrechterhalten. Daneben beeinflussen eine Reihe exo- und endogener Faktoren Verlauf und Schweregrad der Erkrankung.
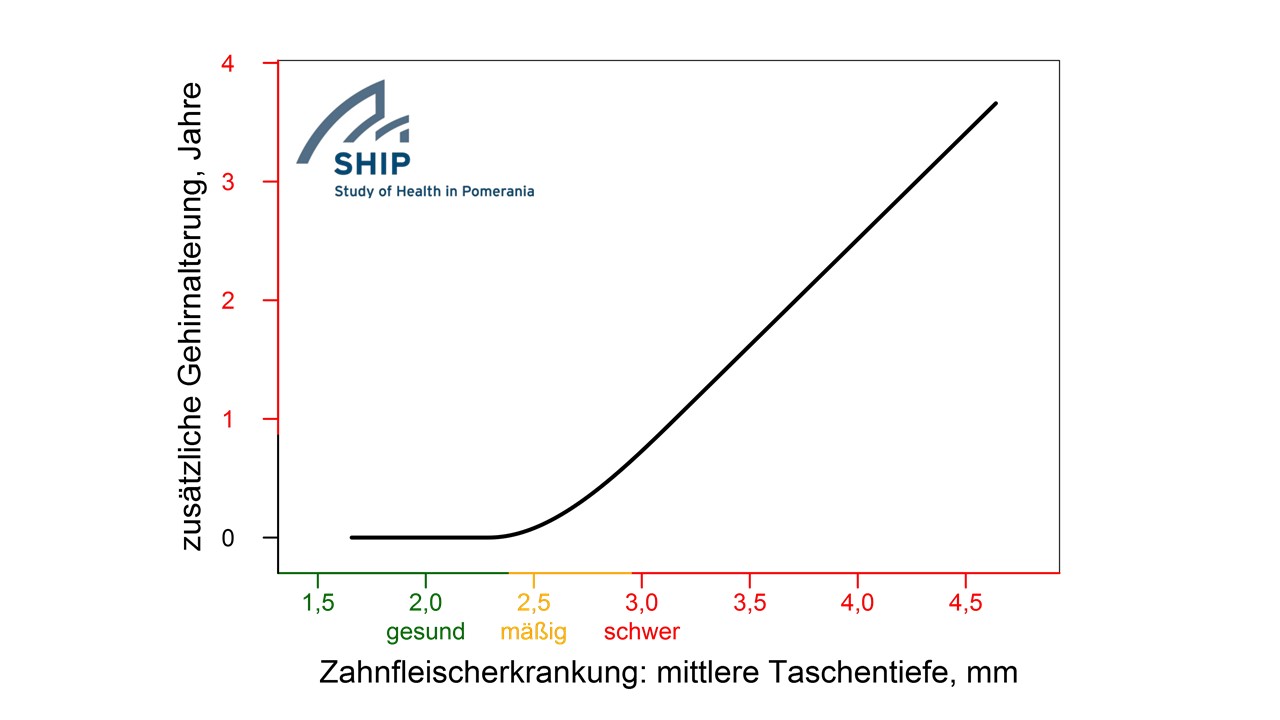
Chronische orale Entzündungen betreffen, wie wir heute wissen, keineswegs nur die Mundgesundheit. Sie führen zu einem systemisch erhöhten Level an proinflammatorischen Mediatoren und über rezidivierende Bakteriämie zu einem direkten Keimtransfer zu den inneren Organen des Körpers. Die Folgen sind Entgleisungen metabolischer Erkrankungen wie Diabetes und Hyperlipidämie, ein erhöhtes Risiko für Atherosklerose, Herz/Kreislauferkrankungen und Insult, eine Begünstigung der Progression neurodegenerativer Krankheiten (M. Parkinson, M. Alzheimer) und gastrointestinale Störungen; um nur einige der negativen Auswirkungen eines destabilisierten oralen Mikrobioms zu nennen.
Mikrobielle Interaktion bestimmt die Pathogenität der Sulkusflora
Die ursprüngliche Annahme, dass ausschließlich bestimmte meist anaerobe oder fakultativ anaerobe Leitkeime als Verursacher und Betreiber der oralen Entzündung in Frage kommen, muss heute durch unser Wissen über das orale Mikrobiom ergänzt und modifiziert werden. Virulenz und pathologisches Potenzial bestimmter Keime hängen nicht nur von deren Anwesenheit im Sulkus oder auf der Schleimhaut ab. Erst Interaktionen zwischen bestimmten Bakterien- und Pilzspezies ermöglichen die Bildung von Biofilmen, welche die Voraussetzung der parodontalen Gewebedestruktion darstellt. Mechanismen wie bakterielle Syn- und Antagonismen sowie Koaggregation fördern Wachstum und Vermehrung potenziell pathogener Arten und ermöglichen im Schutz der zellfreien, organischen Matrix des Biofilms eine optimale Expression von Virulenzfaktoren und Resistenzgenen.
Schlüsselkeim im subgingivalen Biofilm
In der Einteilung parodontal relevanter Keime wird Fusobacterium nucleatum oft nur als mäßig pathogen betrachtet. Dem behandelnden Zahnarzt ist vor allem die Eradikation oder zumindest die Reduktion von aggressiven Mikroorganismen, wie Aggregatibacter actinomycetem comitans, Porphyromonas gingivalis, Treponema denticola, oder Keimen der Prevotellagruppe ein primäres Anliegen. Dennoch kommt gerade F. nucleatum sowohl als Wegbereiter der oralen Entzündung als auch bei deren systemischen Aspekt große Bedeutung zu.
Das Bakterium findet sich, wie die meisten parodontal-aktiven Bakterien, in moderater Menge auch in der normalen gesunden Mundflora. Bei aufrechter Homöostase innerhalb der Biozönose der Mundhöhle besteht Gleichgewicht zwischen den Hart-und Weichgeweben und der Mikroflora. Erst durch einen Shift innerhalb des Mikrobioms in Richtung aggressiver Keime und gleichzeitiger Artenverarmung der mikrobiellen Lebensgemeinschaft kommt es zur Dysbiose. Die potenten Pathomechanismen von Fusobacterium werden dann zu einem zentralen Faktor für die nachfolgenden entzündlich-destruktiven Prozesse.
Voraussetzung für die Zerstörung der Gingiva und der alväolären Knochensubstanz ist die Fähigkeit von Bakterien zur Invasion in tiefere Gewebeschichten. Hier hat Fusobacterium nucleatum eine synergistische Vermittlerrolle zwischen den frühkolonisierenden Keimen der Plaque und hoch aggressiven Keimen.
Durch die Produktion von Adhäsinen kann F. nucleatum sowohl direkt an epitheliale Oberflächen binden als auch zum Brückenbildner zwischen unterschiedlichen Mikroorganismen und Speichelproteinen werden. Fusobacterium nucleatum haftet über ein spezifisches Adhäsin (FadA) direkt an der Wirtszelle. Das Adhäsin ermöglicht ihm die Epithel-/Bindegewebeschranke zu durchbrechen und an Kollagen und Fibroblasten zu binden, Die Moleküle der äußeren Zellmembran (OMPs) von F. nucleatum, wie Fap2 und Rad, sind wichtig für die Zellaggregation. Besonders eines dieser Outer Membrane proteins, nämlich das Porin FomA, fungiert hier als eine Schnittstelle zwischen den Fusobakterien und ihrer Umgebung.
Koaggregation fördert pathogene Mikroorganismen
Fusobacterium zeigt direkte Interaktionen mit parodontal-pathogenen Keimen wie Porhyromonas gingivalis. Es kann Glukose in Form eines intrazellulären Glucans akkumulieren. In nährstoffarmen Medien wird der Traubenzucker dann freigesetzt. Die in Assoziation zu F. nucleatum stehenden Parodontalkeime profitieren unmittelbar davon und werden in ihrem Wachstum und ihrer Vermehrung gefördert. Eine weitere erfolgreiche Koaggregation besteht zu der häufig in tiefen Zahnfleischtaschen präsenten Candida albicans. Fusobakterien haften hier über Oberflächenproteine und Kohlenhydratreste auf den Pseudohyphen der Hefe. Durch die Produktion bestimmter Signalmoleküle, den „Autoinducern“ kann F. nucleatum die bakteriellen Phänotypen im Biofilm steuern und modifizieren.
Neben seiner Vermittlerrolle verfügt der Keim auch selbst über einige wirkungsvolle Virulenzfaktoren. Bei seinem Stoffwechsel entstehen toxische Metaboliten, wie Butyrat, Proprionate und Ammoniumionen, welche die Fibroblastenproliferation des gingvalen Bindegewebes hemmen und so die Abheilung entzündlicher Läsionen behindern. Zusätzlich kommt es zu einer Degradierung der epithelialen Basalmembranen und zu Störungen in der Kollagenbildung und Vernetzung. Der Keim besitzt die Fähigkeit zur Agglutination von Erythrozyten und zur Haemolyse, beides betreibende Prozesse der parodontalen Erkrankung.
Neben diesen vorwiegend die orale Gesundheit beeinträchtigenden Faktoren ist F. nucleatum der am häufigsten an nicht-oralen Infektionen beteiligte orale Keim. Durch sein gewebeinvasives Potenzial wird das Bakterium rasch über die Blutbahn zu diversen Loci des Körpers transportiert, wo es entweder als alleiniger Erreger oder in Kombination mit anderen Keimen schwere Erkrankungen auslösen kann. Sie reichen von septischer Arthritis über Abszesse der Leber und der Tonsillen, infektiöser Thrombophlebitis (Lemierres Syndrom) und Infektionen des Urogenitaltrakts bis zu intrauterinen Infekten während der Schwangerschaft mit hohem Frühgeburtsrisiko. Seine Nachweisbarkeit in atheromatösen Plaques bestätigt die Beteiligung von Fusobacterium an der Progression arteriosklerotischer Erkrankungen.
Besondere Bedeutung gewinnt der Keim durch seine Funktion in krebsassoziierten Biofilmen und seiner Assoziation zu Dickdarmkarzinomen, welche im Teil 2 des Beitrags diskutiert werden.