Oralmedizin kompakt – Update: Patienten in Entscheidungsprozesse einbeziehen und Schmerzen kontrollieren
Parodontitis-Therapie ist ein erfolgreiches Konzept, aber nur wenn Patienten langfristig zu ihren Recall-Terminen (UPT) erscheinen. Das ist sehr häufig nicht der Fall, die Adhärenz-Rate beträgt im ungünstigen Fall nur etwa ein Drittel [1]. Verschiedene Strategien können dazu beitragen, diese Quote signifikant zu verbessern, darunter gute Kommunikation und schmerzvermeidende Behandlungsmethoden. So beurteilten in einer kontrollierten schwedischen Studie Patienten, die sich von ihrem Behandlungsteam „abgeholt“ fühlten, ihre Behandlung unabhängig vom Protokoll positiver.
Kurz und klar
- Patienten brechen Parodontitis-Behandlungen häufig ab.
- Für eine positive Therapiebewertung könnte Patientenbeteiligung an Entscheidungen wichtiger sein als das klinische Protokoll.
- Rauchen und hohe Blutungsindizes zu Behandlungsbeginn sind wichtige Faktoren für Therapiebewertung und klinisches Ergebnis.
- Schmerzarme Therapiemethoden sollten bevorzugt und schmerzmindernde Optionen genutzt werden.
Eine Therapie-Sitzung reicht aus
Bei insgesamt 494 Patienten wurde in einer Therapiegruppe zu Beginn durch intensive Instruktion und Beratung eine gute Mundhygiene etabliert (Plaque-Index <30 Prozent), danach die Ultraschall-Instrumentierung in einer Sitzung durchgeführt [2]. In der anderen Gruppe erfolgten vor der Behandlung nur eine Routine-Mundhygiene-Unterweisung und die Instrumentierung in mehreren Sitzungen. Die Ergebnisse waren nach sechs Monaten in Bezug auf die Mitarbeit in der täglichen Mundhygiene, die objektiv erreichten klinischen Werte und die Patientenzufriedenheit mit Behandlung und subjektivem Erfolg für beide Gruppen vergleichbar [2, 3]. Rauchen und hohe Blutungsindizes zu Behandlungsbeginn hatten wesentlichen Einfluss auf Entzündungswerte und Patientenbewertung [2].
Als signifikanter Faktor für eine positive Beurteilung erwies sich die Frage, ob die Patienten sich in den Entscheidungsprozess für die Behandlung einbezogen fühlten. Der Wert einer solchen „sprechenden“ Medizin und systematischer Maßnahmen zur Steigerung der Adhärenz (Mitarbeit, Recall-Bindung) wird laut Diskussion in der vorgestellten Untersuchung und nach Ergebnissen weiterer Studien, auch aus anderen medizinischen Fachgebieten, bestätigt [2, 4–6].
In einem Übersichtsartikel werden hierzu und zum Thema Patientenzentrierung unter anderem folgende Punkte gelistet (gekürzt) [7]:
- Aufklärung über Ätiologie und Risikofaktoren
- Partizipative Entscheidungsfindung bei Therapie und Schmerzkontrolle
- Motivation zu einem geeignetem Mundhygieneverhalten, bei Bedarf unter Einbeziehung von Angehörigen
- Maßnahmen zur Unterstützung des körperlichen Wohlbefindens (zum Beispiel Behandlung von Mundgeruch, ästhetische Maßnahmen)
Schmerzen vermeiden oder minimieren
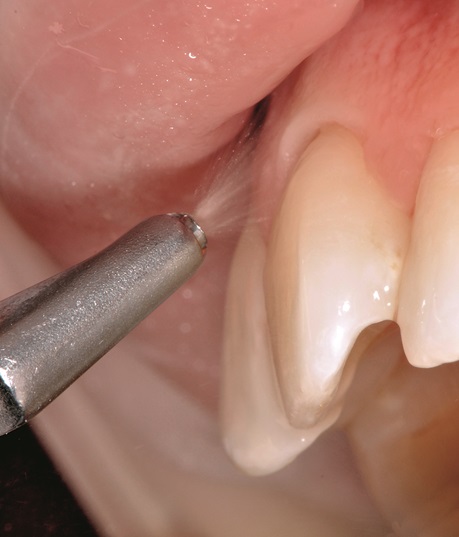
Ein weiterer wichtiger Aspekt der Patientenbindung und damit des Behandlungserfolgs ist die Schmerzvermeidung. Dazu passt, dass Patienten ihre Lebensqualität im Verlauf einer Parodontitis-Therapie zwar insgesamt positiv beurteilen [8]. Die deutlichste Verbesserung erfolgt nach einer supragingivalen Belagentfernung im Rahmen der vorbereitenden Behandlung. Ein kleinerer Effekt ist noch im Anschluss an die subgingivale nicht-chirurgische Therapie messbar [8]. Dieser nimmt nach einer gegebenenfalls notwendigen chirurgischen Behandlung weiter ab [9].
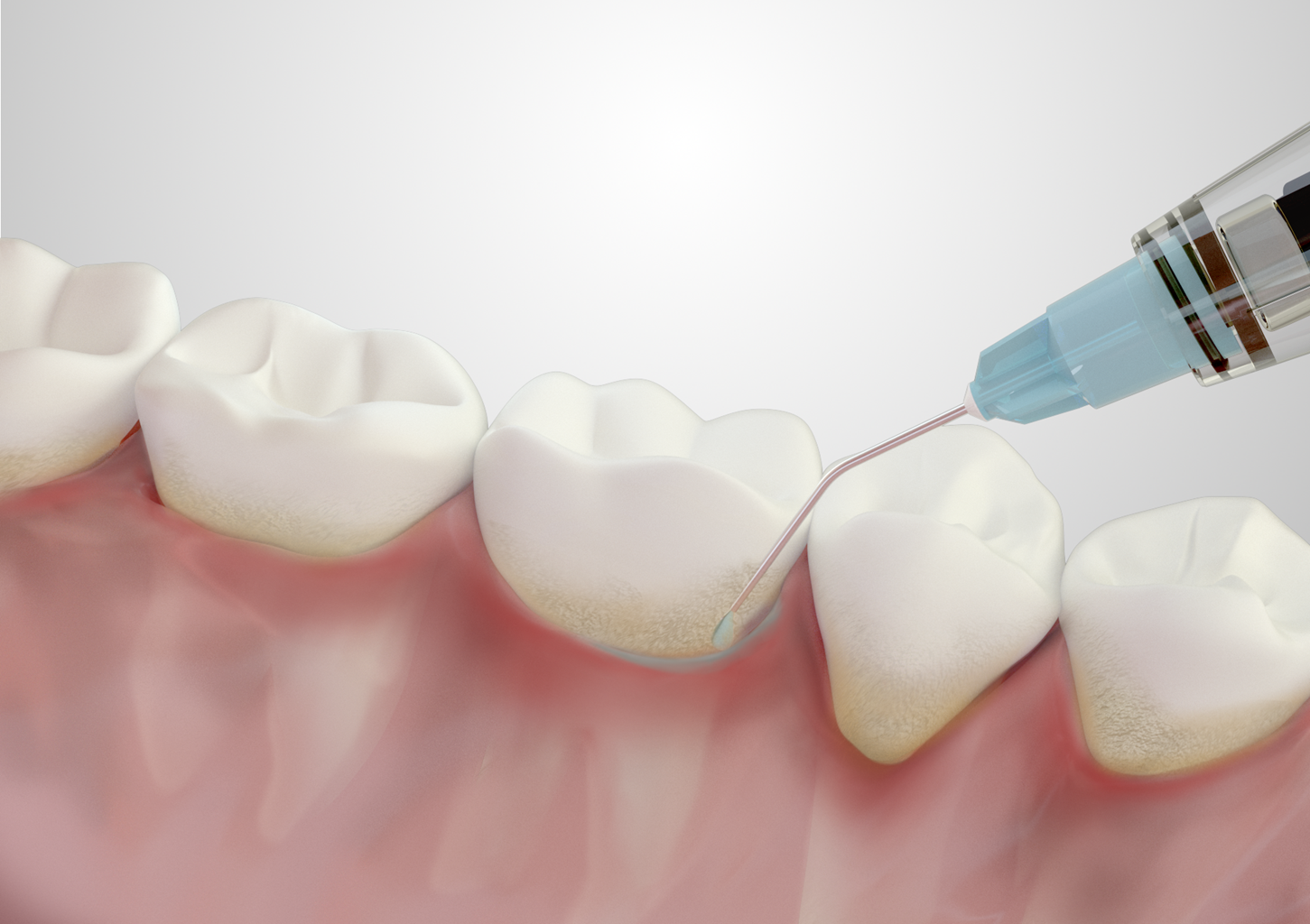
Um Schmerzen zu vermeiden, stehen neben Lokalanästhesie mit injizierbaren Anästhetika verschiedene gelartige Produkte zum Einbringen in die parodontale Tasche zur Verfügung [7]. Weiter besteht vor allem in der Nachsorge (UPT) die Option, Luft-Wasser-Pulver-Systeme mit oder ohne spezielle Aufsätze für tiefere Taschen zu verwenden. Studien liegen hier überwiegend für ein Produktsystem vor, das einen kontinuierlichen Pulverfluss gewährleistet [10–12].
Diskussion und Fazit
Studien zeigen, dass die Mitarbeit von Patienten bezüglich Mundhygiene und Recall-Bindung wesentlich von der Beteiligung an Entscheidungsprozessen abhängt. Die erreichte Therapie-Adhärenz, vermutlich in Verbindung mit reduzierten Risikofaktoren wie schlechter Mundhygiene, Rauchen oder ungünstiger Ernährung bei „aufgeklärten“ Patienten, sind wesentliche Erfolgsfaktoren für die gesamte Therapie. Da sich eine pathologisch relevante Dysbiose über längere Zeiträume von Wochen oder Monaten entwickelt, könnte die Adhärenz als Gesamtkonzept, einschließlich der „Droge Arzt oder Ärztin“, wichtiger sein als Einzelfaktoren wie die Mundhygiene-Qualität [13, 14]. Obwohl dies durch Studien nur schwer nachweisbar ist, dürfte eine – individuell sehr unterschiedliche – Kombination mehrerer Faktoren das Entscheidende sein. Eine besondere und zentrale Rolle spielt wahrscheinlich eine erhöhte Dysbiose- und Entzündungsneigung [15–18]. Die Schwierigkeit besteht nach wie vor darin, betroffene Patienten im Sinne einer Risikodiagnostik sicher zu identifizieren.
In den Konzepten der Bundeszahnärztekammer und der parodontologischen Fachgesellschaften ist das Primat der sprechenden Medizin als Baustein einer risiko-orientierten Therapie bereits berücksichtigt [19, 20]. Wenn zusätzlich alle Möglichkeiten einer schmerzarmen Belagentfernung genutzt werden, sollte die Patientenadhärenz und damit auch die Erfolgsquote von Parodontitis-Behandlungen für jedes Team in einem hohen Prozentbereich liegen. Besser ist da nur noch eine primäre Prävention, noch bevor sich eine Parodontitis überhaupt etabliert hat.
Dr. med. dent. Jan H. Koch, Freising
Hinweis: Der Autor erklärt, dass er folgende Interessenkonflikte hat: Beratung und Lieferung von Beiträgen für die Firma EMS. Dieser Beitrag wurde im Auftrag des ZFV für die dzw erstellt.
Beiträge in der Rubrik Oralmedizin kompakt können nicht die klinische Einschätzung der Leser ersetzen. Sie sollen lediglich – auf Basis aktueller Literatur und/oder Experten-Empfehlungen – die Entscheidungsfindung unterstützen.
Dr. Jan H. Koch
Dr. med. dent. Jan H. Koch ist approbierter Zahnarzt mit mehreren Jahren Berufserfahrung in Praxis und Hochschule. Seit dem Jahr 2000 ist er als freier Fachjournalist und Berater tätig. Arbeitsschwerpunkte sind Falldarstellungen, Veranstaltungsberichte und Pressetexte, für Dentalindustrie, Medien und Verbände. Seit 2013 schreibt Dr. Koch als fester freier Mitarbeiter für die dzw und ihre Fachmagazine, unter anderem die Kolumne Oralmedizin kompakt.
Mitglied seit
7 Jahre 10 MonateLiteratur
[1] Amerio E, Mainas G, Petrova D, et al. Compliance with supportive periodontal/peri-implant therapy: A systematic review. J Clin Periodontol. 2020;47(1):81-100. Epub 20191113.
[2] Liss A, Wennström JL, Welander M, et al. Patient-reported experiences and outcomes following two different approaches for non-surgical periodontal treatment: a randomized field study. BMC Oral Health. 2021;21(1):645. Epub 20211215.
[3] Tomasi C, Liss A, Welander M, et al. A randomized multi-centre study on the effectiveness of non-surgical periodontal therapy in general practice. J Clin Periodontol. 2022;49(11):1092-105. Epub 20220727.
[4] Järvinen M, Stolt M, Honkala E, et al. Behavioural interventions that have the potential to improve self-care in adults with periodontitis: a systematic review. Acta Odontol Scand. 2018;76(8):612-20. Epub 20180725.
[5] Kupke J, Wicht MJ, Stützer H, et al. Does the use of a visualised decision board by undergraduate students during shared decision-making enhance patients’ knowledge and satisfaction? - A randomised controlled trial. Eur J Dent Educ. 2013;17(1):19-25. Epub 20120914.
[6] Newton JT, Asimakopoulou K. Managing oral hygiene as a risk factor for periodontal disease: a systematic review of psychological approaches to behaviour change for improved plaque control in periodontal management. Journal of Clinical Periodontology. 2015;42:S36-S46.
[7] Derman SH. Patientenzentrierte Parodontitistherapie: Was hat sie mit Schmerzkontrolle zu tun? Plaque ‘N Care. 2023;17(1):18-24.
[8] Mendez M, Melchiors Angst PD, Stadler AF, et al. Impacts of supragingival and subgingival periodontal treatments on oral health-related quality of life. Int J Dent Hyg. 2017;15(2):135-41.
[9] Graziani F, Tsakos G. Patient-based outcomes and quality of life. Periodontol 2000. 2020;83(1):277-94.
[10] Donnet M, Fournier M, Schmidlin PR, et al. A Novel Method to Measure the Powder Consumption of Dental Air-Polishing Devices. Applied Sciences. 2021;11(3):1101.
[11] Buhler J, Amato M, Weiger R, et al. A systematic review on the patient perception of periodontal treatment using air polishing devices. Int J Dent Hyg. 2016;14(1):4-14. Epub 20150123.
[12] Ulvik IM, Saethre T, Bunaes DF, et al. A 12-month randomized controlled trial evaluating erythritol air-polishing versus curette/ultrasonic debridement of mandibular furcations in supportive periodontal therapy. BMC Oral Health. 2021;21(1):38. Epub 2021/01/23.
[13] Elkerbout TA, Slot DE, Rijnen ME, et al. Change in oral hygiene behaviour after non-surgical periodontal therapy - A retrospective analyses. Int J Dent Hyg. 2023;21(1):259-71. Epub 20220411.
[14] Zenthofer A, Dieke R, Dieke A, et al. Improving oral hygiene in the long-term care of the elderly--a RCT. Community Dent Oral Epidemiol. 2013;41(3):261-8. Epub 20120929.
[15] Abdulkareem AA, Al-Taweel FB, Al-Sharqi AJB, et al. Current concepts in the pathogenesis of periodontitis: from symbiosis to dysbiosis. J Oral Microbiol. 2023;15(1):2197779. Epub 20230402.
[16] Darveau RP. Periodontitis: a polymicrobial disruption of host homeostasis. Nat Rev Microbiol. 2010;8(7):481-90. Epub 2010/06/02.
[17] Marchesan JT, Moss K, Morelli T, et al. Distinct Microbial Signatures between Periodontal Profile Classes. J Dent Res. 2021;100(12):1405-13. Epub 20210427.
[18] Meyle J, Chapple I. Molecular aspects of the pathogenesis of periodontitis. Periodontol 2000. 2015;69(1):7-17.
[19] Bundeszahnärztekammer. Qualifizierte Prophylaxe in der Zahnarztpraxis. Leitfaden der Bundeszahnärztekammer, 2nd edition. 2 ed2004.
[20] Tonetti MS, Chapple IL, Jepsen S, et al. Primary and secondary prevention of periodontal and peri-implant diseases: Introduction to, and objectives of the 11th European Workshop on Periodontology consensus conference. J Clin Periodontol. 2015;42 Suppl 16:S1-4.